2022年11月30日,肝脏病领域权威期刊《Journal of Hepatology》(欧洲肝脏研究学会会刊,IF=30)在线发表生命科学学院黄赞教授课题组题为“Decreased propionyl-CoA metabolism facilitates metabolic reprogramming and promotes hepatocellular carcinoma”(丙酰辅酶A代谢减少增强代谢重编程促进肝细胞癌发生)的研究论文。
肝细胞癌(HCC)代谢重编程已在基因组、转录组、蛋白质组和代谢组水平上得到表征。一般范式认为糖酵解(Warburg效应)、谷氨酰胺水解、核苷酸和脂肪酸合成的增加促进HCC。相反,HCC在氧化磷酸化、β-氧化和三羧酸(TCA)循环中表现出异质性。HCC如何适应和协调代谢改变的不同方面以支持肿瘤的起始和进展仍然是一个未解决的问题。同时,包括丙酰辅酶A(Pro-CoA) 在内的许多代谢物的改变被认为是HCC诊断和治疗的生物标志物,但在代谢重编程和肝癌发生中的作用尚不清楚。该项研究显示ALDH6A1下调导致Pro-CoA及其衍生物丙酰-左旋肉碱(PLC)的降低与HCC密切相关。功能上,ALDH6A1介导的Pro-CoA代谢抑制了肝癌增殖并破坏肝癌发生;ALDH6A1醛脱氢酶活性对其功能必不可少,而Pro-CoA羧化酶通过消除Pro-CoA而拮抗ALDH6A1功能。机制上,ALDH6A1介导的Pro-CoA代谢影响癌症中枢碳代谢损害能量代谢:ALDH6A1催化产生的Pro-CoA竞争性抑制柠檬酸合酶(CS)活性,降低了TCA循环通量,损害线粒体呼吸和膜电位,导致ATP产能降低。Pro-CoA代谢还产生2-甲基柠檬酸(MCA),模拟Pro-CoA抑制CS活性,损害线粒体呼吸和HCC增殖。这项研究结果表明Pro-CoA、PLC和MCA可能是HCC诊断和治疗的新型代谢生物标志物,Pro-CoA代谢可能为HCC治疗提供潜在靶点。本研究为HCC发生中的代谢重编程提供了新见解,为研发HCC治疗策略提供新思路。

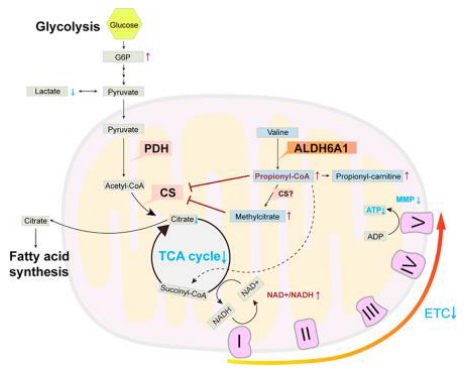
Pro-CoA代谢抑制HCC机理模式图(图源自Journal of Hepatology)
武汉大学生命科学学院孙佳琪博士研究生和武汉植物园丁俊研究员为论文共同第一作者,生命科学学院黄赞教授和基础医学院张鹏研究员为论文共同通讯作者。本研究获得国家自然科学基金面上项目、重大研究计划(培育)项目的资助,得到湖北省肿瘤医院,武汉大学模式动物研究所、中南医院和人民医院的大力协助。
原文链接:https://doi.org/10.1016/j.jhep.2022.11.017